近日,广东省医学科学院聂立铭教授团队在国际顶级期刊《Light: Science & Applications》上发表了一项具有里程碑意义的创新研究,报道了其开发的时空分辨代谢路径跟踪(SRCPT)技术。该技术通过结合非电离的光声断层成像(PACT)与创新的频率分量选择合成孔径聚焦技术(FCS-SAFT),成功实现了对肝肾循环中代谢物清除路径的高精度、实时三维示踪。相比传统成像方法,SRCPT技术不仅消除了辐射风险,还突破了深度和精度限制,为精准医学领域的药物代谢研究提供了全新的工具。这一突破性技术为临床药物在不同生理和病理条件下的代谢路径研究开辟了新路径,并将大力推动精准医学的发展。

近年来,随着精准医学的迅猛发展,深入理解药物在体内清除路径,尤其是在肝脏和肾脏等关键器官中的代谢过程,成为了领域关注的焦点。然而,传统成像技术如PET/CT虽然能够提供清晰的图像,却伴随着辐射风险,且在时空分辨率上存在局限性。这使得药物清除路径的实时、精确监测存在挑战。
针对这些技术难题,由广东省医学科学院光学影像团队开发了一种全新的时空分辨代谢路径跟踪(Spatiotemporally Resolved Clearance Pathway Tracking,SRCPT)方法。该方法结合非电离的光声断层成像技术(Photoacoustic Tomography computed technology,PACT),不仅克服了激光衰减带来的深度成像困难,还通过创新的频率分量选择的合成孔径聚焦技术(Frequency Component Selection based Synthetic Aperture Focusing Technique,FCS-SAFT),极大地提升了三维成像的分辨率,实现了药物代谢路径实时监测。
看得更深、定量更准:
该方法利用创新的动态合成扫描光声技术跟踪监测体内外源探针,使用蒙地卡罗算法计算光在生物体内的光通量分布解决光衰减带来的光声信号定量不准的问题(图1所示),突破了传统成像的深度和精度限制,实现了对肝脏和肾脏等关键器官中药物清除路径的高深度以及高精度观测。该技术不仅避开了辐射风险,同时也还能在深层组织中精确定量药物的代谢过程,为精准医学提供了更可靠的数据支持。

图1 (a)PAT扫描原理及过程,该技术可用于全省器官代谢监测。(b),(c)原始光声影像。(d), (e) 蒙地卡罗算法计算得到光通量。(f),(g)经过校准的光声影像。
高时空分辨三维药物代谢示踪:
为了验证该技术的有效性,研究团队对临床药物米托蒽醌(Mitoxantrone)的清除路径进行了深入研究,并针对代谢过程进行了高时空分辨三维成像,对于环形超声阵列PACT的三维成像,该方法利用合成孔径聚焦技术(Synthetic Aperture Focusing Technology,SAFT)解决了远离焦点区域的失焦问题,并且分离小鼠三维数据中低频信号来对药物代谢信息进行准确、快速显影(图2所示)。研究结果清楚地显示,在正常情况下,米托蒽醌主要经肝脏代谢,少量通过肾脏清除。而当肝功能受损时,肝脏的代谢能力显著降低,药物的半衰期大幅延长,表明该药物在肝脏受损时清除效率显著下降。在这一发现为临床药物在不同生理和病理条件下的清除路径研究提供了全新的视角。

图2 (a)FCS-SAFT算法的原理。(b)原始光声三维数据。(c) 经过算法处理的三维数据。(d)三维数据中的高频血管成分。(e)三维数据中的低频组织以及探针信号
生物大分子的清除追踪:
该团队在研究中还应用SRCPT技术监测了免疫球蛋白G(Immunoglobulin G,IgG)在肾脏中的动态沉积过程(图3所示)。结果表明,在急性肾损伤模型中,IgG的沉积量随着肾损伤程度的加重而显著增加,清除效率显著下降。这一发现不仅揭示了肾脏在不同损伤程度下的功能变化,还为今后开发针对肾脏疾病的治疗方法提供了重要依据。
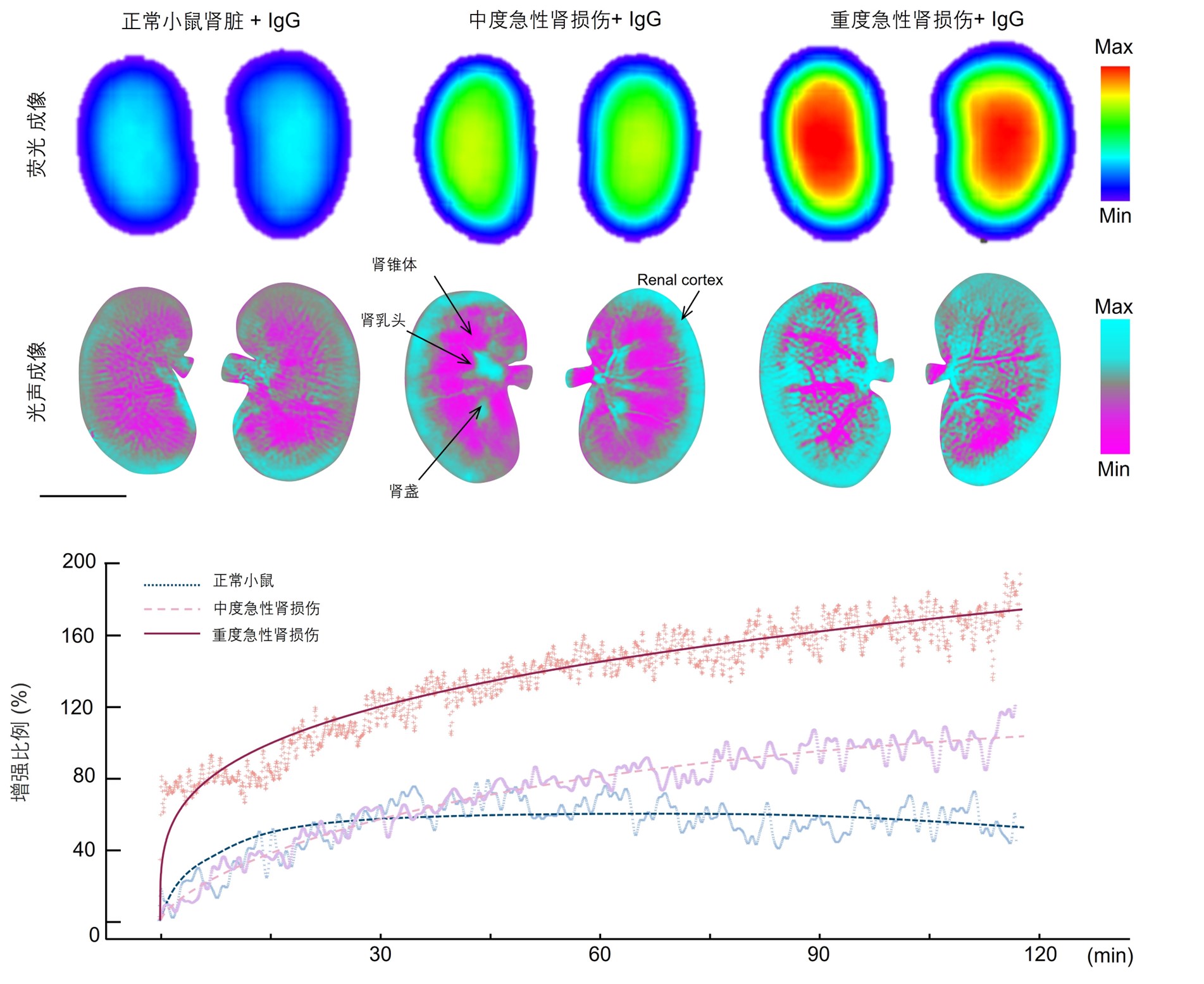
图2 (a)正常小鼠以及不同程度急性肾损伤模型小鼠的IgG沉积情况。(b)通过SRCPT监测得到的代谢曲线
创新与亮点:
- 合成孔径聚焦技术的突破: 团队开发的FCS-SAFT算法通过频率分量选择,有效提升了三维成像的横向和纵向分辨率,清晰展示了药物在各个器官中的清除路径。
- 多器官实时监测: 通过SRCPT技术,研究团队能够实时监测药物在肝脏和肾脏中动态清除过程,为临床药物的代谢研究提供了重要工具。
该研究不仅在技术上实现了重大突破,还为药物代谢研究提供了新的思路,展示了精准医学在药物代谢路径研究中的巨大潜力。未来,SRCPT技术有望在更多药物研究中得到广泛应用,推动精准医学的发展,为患者带来更精准的治疗方案。
光学分子影像实验室(聂立铭教授团队)简介:

聂立铭教授团队是一支由基础科学、影像工程和临床医学等多学科专家组成的约30人团队,充满了创新活力。团队通过自主研发和联合开发,构建了一个覆盖全尺度的多模影像平台,为本次课题的实施提供了坚实的技术保障。这一平台不仅为科研工作的深入开展奠定了基础,也为光学影像研究的前沿探索开辟了新的路径。


